Geschichte
Die Ägypter beherrschten schon vor 4 000 Jahren das Färben mit Indigo und die Phönizier gelangten durch ihre Fertigkeit, mit Purpur zu färben, zu Wohlstand. Bedenkt man, dass in einem komplizierten Verfahren aus 12000 Schnecken nur 1 g Farbstoff gewonnen werden kann, so wird verständlich, warum im Altertum purpurgefärbter Stoff als Zeichen extremen Reichtums galt.
Bis zur Mitte des vorigen Jahrhunderts - ausschließlich natürliche Farbstoffe
1856- Engländer Perkin stellte bei dem Versuch, aus Anilin das Malariamedikament Chinin zu synthetisieren, einen brauchbaren Farbstoff her, den er Mauvein (engl.: malvenfarben = hellviolett) nannte. Dies löste eine stürmische Entwicklung aus und in den folgenden Jahren wurde in rascher Folge aus dem im Steinkohlenteer enthaltenen Anilin[1] eine Reihe von Farbstoffen hergestellt, die billiger und lichtechter als Naturfarbstoffe sind (sogenannte Anilin- oder Teerfarben).
Verwendung:
zum Färben von Faserstoffen, Pelzwerk, Leder, Holz, Papier, Nahrungs- und Genußmitteln, Eloxalschichten, mikroskopischen Präparaten;
zum In-Masse-Färben von Plasten, Elasten, Wachs, Seife u.dgl.;
für Druckfarben, Schreibpasten und -flüssigkeiten, Schreibmaschinen- und Druckerfarbbänder, lasierende (durchscheinende) Anstriche;
zur Herstellung von Pigmenten (durch "Verlackung" mit einem Substrat[2]);
in Reproduktions-, z.B. Lichtpaustechniken; in der Farbfotografie und als fotografische Sensibilisatoren;
als chemische Indikatoren u.v.a.m.
Licht und Materie
Elektromagnetische Strahlung im Wellenbereich von 380 bis 780 nm bewirkt im menschlichen Auge einen Lichteindruck. Licht größerer Wellenlänge (Infrarot = Wärmestrahlen) kann nur von unserer Haut wahrgenommen werden, für kürzer welliges Licht (Ultraviolett) haben wir kein Sinnesorgan, wir merken diese Strahlung erst durch ihre schädigende Wirkung (Sonnenbrand).
Absorbiert ein Stoff einen Teil des sichtbaren Lichts, so erscheint er farbig. Man beobachtet die Mischfarbe der verbleibenden Spektralfarben. Diese Mischfarbe wird auch Komplementärfarbe des absorbierten Lichts genannt. Stoffe, die nur außerhalb des sichtbaren Bereiches absorbieren, sind farblos. Glas absorbiert z. B. nur im ultravioletten Bereich.
Alle Farben des Spektrums ergeben zusammen als Farbeindruck weiß!
Theorie der Farbigkeit:
Wie kann ein Stoff Licht absorbieren?
Die Energie des Lichts hängt von der Frequenz ab: Kurzwelliges (blaues) Licht ist energiereicher als langwelliges (rotes) Licht.
Es existieren in den Molekülen ebenso wie in den Atomen für die Elektronen nur ganz bestimmte mögliche Energiezustände. Normalerweise befinden sich alle Elektronen auf dem niedrigstmöglichen Niveau (Grundzustand).
Das Licht vermag die Elektronen in einen höheren Energiezustand zu heben. Bei der Bildung von sigma- und π-Orbitale, entstehen außerdem noch die so genannten Antibildenden Molekülorbitale; sigma* und π*. Diese haben eine höhere Energie als sigma und π-Orbitale und sind deshalb meistens nicht mit Elektronen besetzt. Bei der Energieaufnahme können die π-Elektronen in die antibindende Sternorbitale springen. Die dafür nötige Energie entnehmen sie dem sichtbaren Licht. Die dazu gehörige Wellenlänge verschwindet aus dem Spektrum des weißen Lichtes und man sieht die so genannte Komplementärfarbe. Die Elektronen fallen aus den π*-Orbitalen über mehrere Stufen zurück in ihr altes π-Orbital und geben dabei die Energie als Infrarotstrahlung wieder ab.
Also ist ein Stoff farbig, wenn das sichtbare Licht genügt, um das höhere Energieniveau zu erreichen. Also ist Farbigkeit die Fähigkeit aus dem sichtbaren Bereich des Spektrums einen bestimmten Wellenbereich zu absorbieren.
Und Seitengruppen können die Eigenschaften der Farbstoffe beeinflussen!
Chromophore
Es gibt Atomgruppen, die imstande sind, einem Molekül Farbe zu verleihen. Sie werden Chromophore genannt.
Chro|mo|phor ["Farbträger"] der; -s, -e: Atomgruppe organischer Farbstoffe, die für die Farbe des betreffenden Stoffes verantwortlich ist (Chem.).
Wichtige Chromophore sind
- die Azogruppe - N = N - und
- die Nitrogruppe - NO2
Sie sind häufig an aromatische Systeme gebunden.
Chromophore (chromophore Gruppen) verschieben die Lichtabsorption organischer Moleküle so, daß (oft erst bei mehrfachem Vorhandensein) Farbigkeit hervorgerufen wird.
Auxochrome Gruppen
Eine farbvertiefende Wirkung haben Atomgruppen mit freien Elektronenpaaren:
z. B.:
- NH2 - (Aminogruppe)
- OH (Hydroxygruppe)
- O – CH3
- NR2 R ... Alkylrest
Diese Elektronen sind in das delokalisierte System miteinbezogen. Solche Gruppen nennt man auxochrom.
au|xo|chrom [...krom]: eine Farbvertiefung od. Farbänderung bewirkend (von bestimmten chem. Gruppen; Chem.).
Auxochrome (auxochrome Gruppen) bewirken neben einer weiteren Verschiebung der Lichtabsorption eine beträchtliche Erhöhung der Farbintensität und ermöglichen häufig erst das Haften des Farbstoffes am Färbegut.
Anforderung an Farbstoffe:
Mit den Farbstoffen sollte man schöne bzw. gewünschte Farben herstellen können. Sie sollten chemische Beständigkeit vorweisen können. Und sie sollten Lichtecht sein. Dabei unterscheidet man zwischen zwei Gruppen. Einmal die wasserlöslichen Ausgangstoffe, werden zum färben von Textilien verwendet. Und einmal die Pigmente, das sind unlösliche, pulverisierte Farbstoffe, die durch Bindemittel aufgeklebt werden. Sie werden als Druckfarben oder Lacke verwendet.
Die über 500 technisch in größeren Mengen verwendeten Farbstoffe lassen sich auf wenige Grundstrukturen zurückführen:
Azofarbstoffe(Anilinfarbe)
Mehr als die Hälfte gehört in die Gruppe der Azofarbstoffe (azote (frz.): Stickstoff). Ihr charakteristisches Merkmal ist die Azogruppe N= N. Sie ist die zahlenmäßig größte Farbstoffklasse. Wegen der einfachen, meist in Wasser verlaufenden Synthese und den nahezu unbegrenzten Variationsmöglichkeiten bei der Auswahl von Ausgangsprodukten ist diese außerordentlich große Vielfalt von Azofarbstoffen möglich. Durch Verwendung von Ausgangsstoffen mit verschiedenen chromophoren und auxochromen Gruppen sind Azofarbstoffe in fast allen Farben herstellbar. Ihre Zahl wird noch dadurch erhöht, dass ein Farbstoffmolekül mehrere Azogruppen enthalten kann.
Unter den natürlich vorkommenden Farbstoffen sind dennoch keine Azoverbindungen bekannt. Sie werden nur synthetisch hergestellt und stellen nach Zahl und auch Produktionsmenge die größte Gruppe synthetischer Farbstoffe dar. Je nach Anzahl der N=N - Gruppen spricht man von Mono-, Dis-, Tris- usw. Azofarbstoffen.
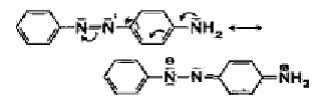 Solche einfachen Systeme absorbieren im blauen Bereich und erscheinen daher gelb. Durch gezielten Einbau von Auxochromen, farbvertiefende Gruppen, wie - OH, - NH 2 erreicht man eine Änderung der Elektronenstruktur und dadurch ein verändertes Lichtabsorptionsverhalten der gebildeten Farbstoffmoleküle, so dass der gesamte sichtbare Bereich durch die verschiedenen Azofarbstoffen abgedeckt werden kann.
Solche einfachen Systeme absorbieren im blauen Bereich und erscheinen daher gelb. Durch gezielten Einbau von Auxochromen, farbvertiefende Gruppen, wie - OH, - NH 2 erreicht man eine Änderung der Elektronenstruktur und dadurch ein verändertes Lichtabsorptionsverhalten der gebildeten Farbstoffmoleküle, so dass der gesamte sichtbare Bereich durch die verschiedenen Azofarbstoffen abgedeckt werden kann.
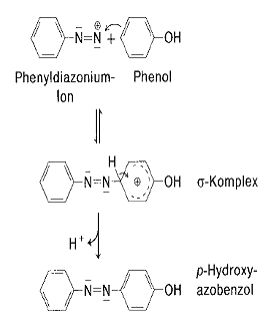
Im Allgemeinen erfolgt die Darstellung eines Azofarbstoffes durch Reaktion zweier Komponenten, der Diazotierung (Primäre aromatische Amine werden mit Natriumnitrit-Lösung in das Diazoniumsalz umgewandelt) und der Azokupplung [Diazoniumlösungen werden mit Phenolen oder aromatischen Aminen zur Reaktion gebracht (Kupplungsreaktion)].
Auch auf der anwendungstechnischen Seite erhält man durch Molekülstrukturänderungen Azofarbstoffe, die zu den anionischen oder kationischen Farbstoffen, den Beizen- oder Direktfarbstoffen, sowie den Reaktiv- oder Dispersionsfarbstoffen gehören. Darstellungsschema eines Azofarbstoffes: Im allgemeinen erfolgt die Darstellung eines Azofarbstoffes durch Reaktion zweier Komponenten, der Diazo- und der Kupplungskomponente.
Anthrachinonfarbstoffe
Anthrachinonfarbstoffe haben besonders brilliante Farbtöne und hervorragende farbtechnische Eigenschaften.
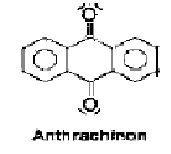
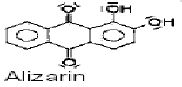
Eine wichtige Farbstoffklasse leitet sich vom Anthrachinon ab, dessen Molekülarchitektur es als günstiges Chromophor ausweist. Das Absorptionsmaximum des Anthrachinons selbst liegt im nahen UV-Bereich. Durch Substitution mit elektronenliefernden Auxochromen
(-OH, -NH) verschiebt sich die Lichtabsorption in den sichtbaren Bereich. Alizarin gehört mit zu den wichtigsten Anthrachinon-farbstoffen.
 |
 |
 |
|---|
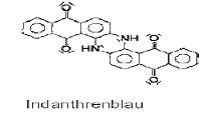
Eine Reihe weiterer technisch wichtiger Anthrachinonfarbstoffe sind die Indanthren-farbstoffe, die zu den Küpenfarbstoffen zählen. Indanthrenblau war der erste Vertreter dieser Gruppe.
Triphenylmethanfarbstoffe
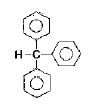
Die Triphenylmethanfarbstoffe sind kationische Abkömmlinge des farblosen Triphenylmethans. Mindestens zwei der Benzolkerne sind mit auxochromen bzw. antiauxochromen Gruppen substituiert, so dass eine weitere Delokalisation der π-Elektronen über die p-Orbitale des zentralen sp3-hybridisierten Kohlenstoffatoms erfolgen kann. Durch Aufstellen mesomerer Grenzformeln kann dies verdeutlicht werden.
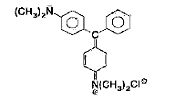
Bekannteste Vertreter dieser Farbstoffklasse sind Malachitgrün und Kristallviolett. Kristallviolett wird unter anderem dazu verwendet, kohlefreie Durchschreibepapiere herzustellen und wird durch Kondensation von Michlers Keton (4,4-Bisdimethylamino-benzophenon) mit Dimethylanilin im saurem Medium gewonnen. Das Malachitgrün ist ein bedeutender Bürofarbstoff. Triphenylmethanfarbstoffe haben einen weiten Anwendungsbereich:
- Phenolphthalein wird z.B.: als Säure-Base-Indikator verwendet.
- Fluorescein ist ungiftig und wird, da seine Lösungen intensiv grün fluoreszieren, Badesalzen zugegeben. Da es auch noch in geringsten Mengen nachweisbar ist, verwendet man es, um den Verlauf unterirdischer Gewässer (z. B. in Karstgebieten) festzustellen.
Indigoide Farbstoffe
Der bekannteste Farbstoff dieser Klasse ist das Indigo, von dem seit mehr als 130 Jahren die Strukturformel bekannt ist. Mit Indigo haben aber schon die alten Ägypter lange vor Christi gefärbt. 1897 wurde erstmals das Indigo auf synthetischem Wege hergestellt. Heute verschmilzt man Natrium-N-phenylgylcin mit Natriumamid und oxidiert das erhaltene Indoxyl mit Luftsauerstoff zu Indigo. Die Produktionsmengen sind heutzutage eher gering. Dagegen wird das Thioindigo, ein roter Farbstoff, in großen Mengen synthetisiert.
Saure Farbstoffe
Die anionischen Farbstoffe enthalten Sulfongruppen und bilden eine salzartige Bindung mit den basischen Aminogruppen von Woll-, Seiden- oder Polyamidfasern.
Basische Farbstoffe
Bei den kationischen Farbstoffen werden basische Gruppen eingebaut und bilden ebenfalls eine salzartige Bindung mit den sauren Gruppen der Faser. Diese Farbstoffe eignen sich zum Anfärben von Wolle, Seide und Polyacrylnitrilfasern.
Carotinoide à Sie haben eine gelb bis rote Farbe. Ihr charakteristisches Merkmal ist die lange Kette zwischen zwei Benzolringen
Chlorophyll à Sie haben eine grüne Farbe. Ihr charakteristisches Merkmal ist das Mg in der Mitte, ganz viele Benzolringe herum
Flavonoide à Sie haben eine tiefrote Farbe. Ihr charakteristisches Merkmal ist ein O im Ring